近日,中國科學院廣州生物醫藥與健康研究院(以下簡稱“廣州健康院”)王金勇研究員團隊在Journal for ImmunoTherapy of Cancer雜志在線發表了題為“CD33KO-CD33-mesothelin loop CAR design avoids fratricide and improves efficacy of iNK cells against acute myeloid leukemia”的研究論文。該研究針對間皮素(MSLN)和CD33靶點雙陽性的急性髓系白血病(AML)設計了環形雙靶點嵌合抗原受體(CD33-MSLN Loop CAR,Loop CAR),并基于臍帶血NK細胞(UCB-NK)或人多能干細胞(hPSCs)誘導的NK(iNK)細胞制備出Loop?CAR-NK或Loop?CAR-iNK細胞。Loop?CAR-NK細胞能夠有效殺傷AML細胞。研究還進一步通過在hPSCs中敲除CD33基因解決了Loop?CAR-iNK細胞因靶向自身CD33抗原分子而引起的“自相殘殺”問題。該研究為AML細胞治療新策略提供理論和技術依據。
AML患者通常年齡較大,不適合進行自體免疫細胞改造治療。開發異基因CAR-NK細胞療法治療AML是重要的探索方向。目前,過繼輸注NK細胞治療AML的研究已廣泛開展。其中,CD33 CAR-NK細胞已在復發/難治性AML治療中展現出初步的療效與安全性。MSLN抗原在部分AML患者中高表達,成為AML治療的潛在靶點。為了提高CAR-NK細胞對MSLN+?AML的治療效果,研究團隊構建了同時靶向CD33和MSLN的“雙導航”Loop CAR,然后利用逆轉錄病毒感染UCB-NK細胞制備出Loop CAR-NK細胞。實驗證明,Loop CAR-NK細胞對CD33+MSLN+ AML細胞系和患者原代AML細胞的殺傷能力顯著優于單靶點CAR-NK細胞。scRNA-seq分析顯示,與單靶點CAR-NK細胞相比,被腫瘤細胞刺激后的Loop CAR-NK細胞展現出更強的激活狀態和細胞毒性活性。
hPSCs來源的iNK細胞質量均一、可現貨式供應,有希望成為人體組織來源NK細胞的替代來源。但UCB-NK細胞和hPSCs來源的iNK細胞均會表達CD33,這使得靶向CD33的CAR-NK細胞會互相攻擊,即“自相殘殺”,導致其擴增能力和活性受損。為了解決這一問題,團隊利用基因編輯技術,在hPSCs中敲除CD33基因構建了CD33KO-hPSCs,再導入Loop CAR構建了CD33KO-Loop CAR-hPSCs,利用課題組前期開發的hPSCs再生iNK技術(Huang Dehao,et al. Cell Discovery,2022)最終誘導分化產生CD33KO-Loop?CAR-iNK細胞。實驗證明,CD33KO-Loop CAR-iNK細胞的擴增能力恢復正常,對CD33+MSLN+AML細胞的殺傷活性也進一步提升。此外,CD33KO-Loop CAR-iNK細胞在細胞系來源的異種移植腫瘤和人源腫瘤異種移植模型中,也展現出更優越的抗腫瘤效果,并顯著延長荷瘤小鼠的生存期。
廣州健康院客座王金勇研究員和北京干細胞與再生醫學研究院胡房曉副研究員為該論文的共同通訊作者。廣州健康院博士后王瑤和博士生鄭秀娟為該論文的共同第一作者。本研究的合作者還包括廣東省人民醫院杜欣教授和李敏明主治醫師,中國醫學科學院血液病醫院(中國醫學科學院血液學研究所)竺曉凡教授、楊文鈺教授和胡甜園副研究員,浙江大學第二附屬醫院錢文斌教授,以及同濟大學醫學院梁愛斌教授。本研究在國家重點研發計劃,國家自然科學基金和國家衛健委四大慢病重大專項等項目支持下完成。
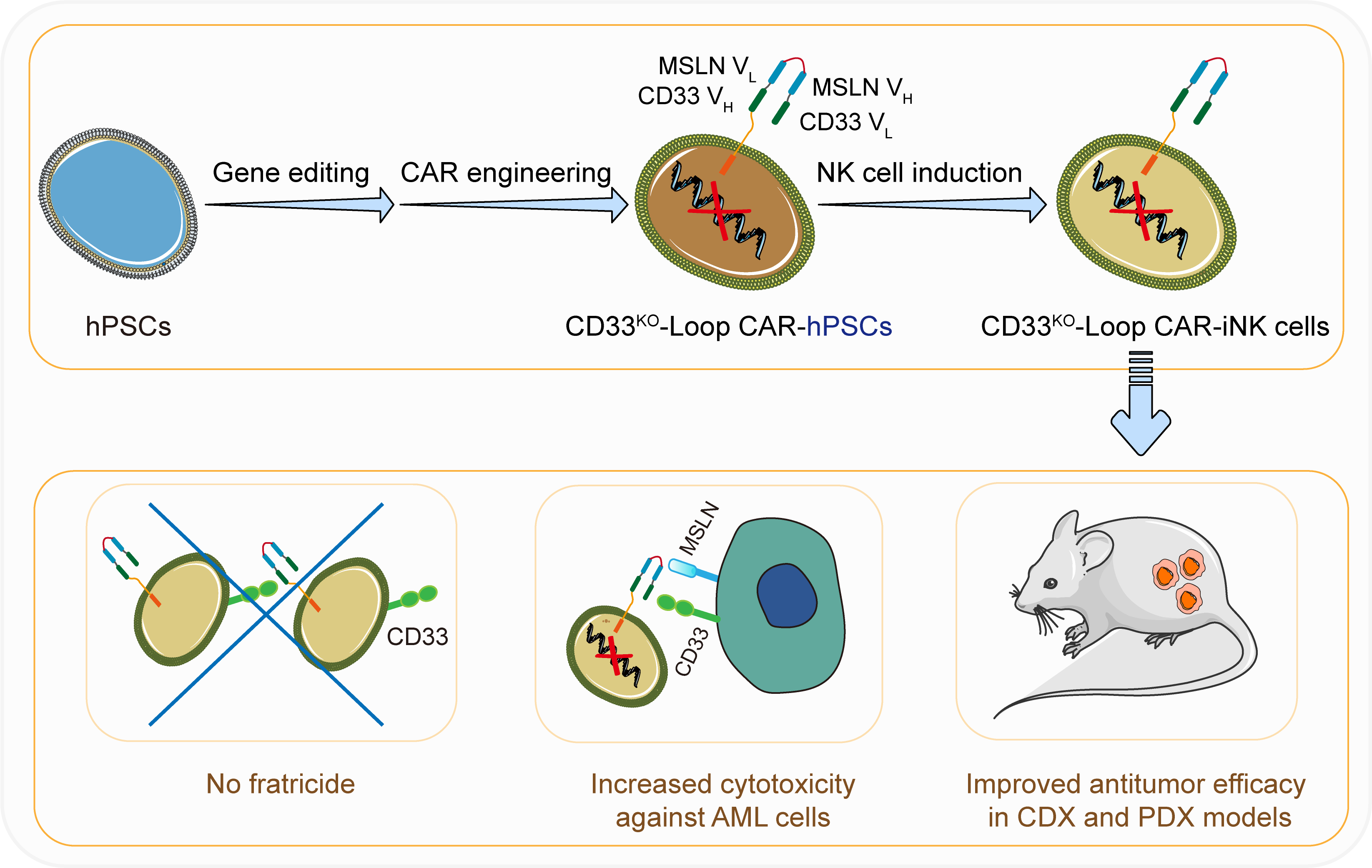
圖1 CD33KO-CD33-MSLN Loop CAR-iNK細胞精準靶向治療急性髓系白血病
附件下載:


